L’action des virus est facilitée et renforcée par les maladies et les parasites déjà dans la colonie
On sait les problèmes de santé de nos abeilles et on connaît les principaux virus qui les attaquent. Ils se transmettent verticalement, des parents aux descendants, et horizontalement, tantôt directement par simple rencontre ou contact dans l’univers surpeuplé de la ruche, ou même par trophallaxie, tantôt indirectement des insectes aux fleurs puis des fleurs à d’autres insectes. Ces virus passent également à d’autres pollinisateurs, solitaires ou sociaux. Varroa destructor, l’acarien parasite des abeilles, les transmet également. La nocivité de ces virus est rendue plus efficace lorsque les insectes sont en état de faiblesse anormale et que leur immunité naturelle est déjà attaquée par la rémanence des pesticides ou l’action de Varroa. Inversement, cette malfaisance renforcée pourra se combiner aux fléaux déjà présents.
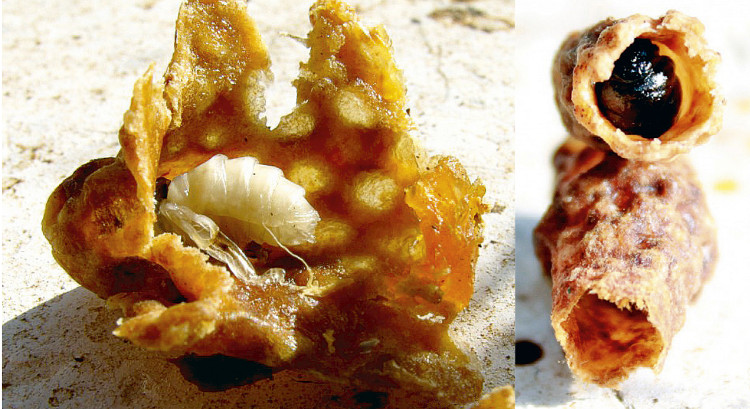
Les nombreux virus connus de l’abeille accélèrent les mortalités
Chez nos abeilles mellifères, le groupe le plus important est celui des virus à ARN simple brin de polarité positive qui inclut des Iflaviridae (DWV ou virus des ailes déformées, virus du couvain sacciforme, virus de la paralysie lente de l’abeille ou SBPV), des Dicistroviridae (virus de la reine noire ou Black Queen Cell Virus, présent surtout en Afrique du Sud – regardez les excellentes photos sur beeinformed.org et accessoirement la fiche Wikipedia « Virus de la paralysie aiguë ABPV » et ses cousins israélien et KBV ou virus de l’abeille du Cachemire). On se rappellera que ces deux derniers virus en particulier, ABPV et KBV (mais les autres aussi sans doute), sont également très présents et actifs dans les colonies de bourdons Bombus, en particulier dans les deux espèces les plus fréquentes chez nous, soit le bourdon terrestre ou « cul blanc » et chez le bourdon des pierres ou « cul brun » (pourquoi diable ce nom ? En fait, B. lapidarius est tout noir avec un arrière-train orange !). N’oublions pas d’autres familles de virus comprenant celui de la paralysie chronique et celui du lac Sinaï, etc.
Les virus semblent être plus présents et on ne sait pas encore les soigner directement

Est-ce qu’on les détecte mieux ? Se seraient-ils plus développés dans le cadre du CCD (syndrome d’effondrement des colonies) dont on a beaucoup parlé il y a 10 ou 15 ans ? Ou bien avec l’invasion de Varroa, comme le virus des ailes déformées ? Ce qui est certain, c’est que les professionnels du « Mais non, ce n’est pas la faute des pesticides », dont nous parlons dans un autre article à paraître ici, ont voulu en faire un argument de leur rhétorique il y a une dizaine d’années. Mais l’existence seule des virus et ce développement régulier nous posent un vrai problème. Dans ce contexte, l’indication d’une piste de blocage possible des virus est d’importance ! Pour l’instant, on se contente de désinfecter les outils et le matériel en passant d’une ruche à l’autre.
Pour se défendre seul, les mécanismes existent déjà
Si le paragraphe suivant est un peu ésotérique, reprenez votre manuel de SVT ou relisez cette page sur le « système immunitaire », par exemple, ou passez vite.
L’évolution a doté les abeilles mellifères de plusieurs mécanismes de défense antiviraux (comme c’est le cas de tous les autres organismes vivants), dont des voies (pathways) de réaction immunitaire conservées classiques (Toll, Imd, JACK/STAT). Si vous voulez devenir généticien ou virologue, allez voir la page pathways for immune response to pathogens. Sinon, continuons.
D’autres mécanismes de défense sont déclenchés par ARN bicaténaire (ARNds). Mais en plus, les analyses de transcriptome impliquent l’action antivirale de diverses réactions de stress qui ont déjà été notées dans diverses études. La transcriptome désigne l’ensemble des gènes exprimés par la cellule à un instant donné ; les analyses ont été faites sur des abeilles infectées par un virus.
Parmi ces dernières réactions figure notre fameuse réaction au choc thermique (HSR ou Heat Shock Response). Mentionnons quand même, avant de revenir à ce choc thermique, que, à l’inverse de beaucoup d’organismes (oserions-nous dire « plus simples » ?), le superorganisme, le peuple de chaque colonie d’abeilles mellifères, a lui aussi des mécanismes de défense immunitaire sociaux, comme le policing et la collecte des larves mortes malades, la récolte de propolis (?), voire le maintien d’une température plus élevée (référence ci-dessous en rubrique Sources).
Le comportement « hygiénique » ou « nettoyeur » des colonies (et de certaines plus que d’autres) fait partie aussi de ces mécanismes sociaux qui réduisent par exemple l’infestation des varroas et donc des virus que ceux-ci transmettent.
Nous avons récemment parlé du choc thermique pour les poissons et contre la COVID-19
Par analogie avec le « bon bol d’air » dont certains apiculteurs autrichiens font bénéficier leurs clients qui ont des problèmes et des maladies respiratoires, mais surtout en partant du « choc thermique » dont se servent des biologistes pour lutter contre les virus qui attaquent les populations des piscicultures, nous avions publié deux petits articles dans les revues de presse d’Abeilles & fleurs de Mai 2020 et d’Avril 2021. On y a rajouté une vidéo de propagande qui explique l’utilisation des inhalations comme moyens de prévention et de soins ainsi qu’un spot concernant l’Inde.
Nous informions alors de la proposition faite par une petite équipe autour de ce biologiste marin qui, depuis 15 ans, pratique « l’hyperthermie » : en présence du pathogène, il soumet les poissons à des chocs de température, très proches de la température létale mais de très courte durée, répétés jusqu’à l’arrêt ou la réduction sérieuse des mortalités. Il proposait simplement de tester la méthode, sous forme d’inhalations de vapeur d’eau chaude, sans ajout aucun, par les malades en suspicion de COVID-19. Un lecteur nous a alors communiqué la référence d’une étude récemment parue dans une revue spécialisée, qui concerne le traitement de plusieurs virus des abeilles par ce même choc thermique et qui nous avait échappée. Mais il en est tant et dans tant de revues !
La chaleur agirait surtout sur le système immunitaire
La chaleur n’attaque évidemment pas directement les virus, car la température à atteindre pour les détruire est incompatible avec ce que peuvent supporter les cellules. C’est très vraisemblablement l’effet sur le système immunitaire inné qui est le plus important car, ses capacités étant surexprimées par la température, il va mobiliser toutes les voies cellulaires pour régler lui-même le problème. Cette excitation à la surexpression des heat shock proteins, ces protéines anti-stress conservées par l’évolution depuis les bactéries jusqu’aux humains (nos biologistes appellent ce processus un conserved immune response pathway), serait la clé des résultats. Là encore, ces résultats sont statistiques et non binaires (nous sommes dans le vivant et nos poissons ne sont pas des machines). Ainsi, un exemple cité pour une espèce de poissons mentionnait un taux de survie remonté de 10 % à 60 % par ces simples chocs thermiques.

A Bozeman (Montana), le choc thermique appliqué aux abeilles
Trois chercheurs de l’université d’Etat du Montana, spécialisés en pathologie des plantes et en santé des abeilles, en immunologie et microbiologie, ont donc entrepris de soumettre les bestioles à un petit coup de chaud : pratiquement, cela consistait à les maintenir à 42°C pendant quatre heures. On sait que les « chauffeuses », les ouvrières qui vont couver le couvain (œufs, larves et pupes), peuvent parfois monter jusqu’à cette température (mais pas au dessus) quand elles remplissent leur fonction. Mais, bien que ravitaillées par les « pompistes », pour ne pas perdre de temps de travail, nos meilleures travailleuses de choc ne maintiennent pas leur activité de chauffe (en activant les muscles de leur thorax) au-delà d’une demi-heure (relire POUR LES “CHAUFFEUSES”, RIEN NE VAUT UN BON POMPISTE). Les abeilles soumises au traitement de nos chercheurs auront donc bien un vrai choc, même si nous restons en dessous des températures létales.
Trois tests distincts
En l’occurrence, on sélectionne de jeunes abeilles (moins d’une heure après l’éclosion), on les maintient à 32°C, on les anesthésie à froid (10 min à 4°C) pour leur injecter dans le thorax une dose bien calculée (pour que l’infection se développe normalement durant le cycle de l’expérience) d’un virus bien connu, le virus Sindbis (SINV). Ce mode d’infection correspond bien à la transmission des virus par notre acarien préféré et il garantit l’homogénéité de la dose. Les piquées récupèrent à nouveau (6 heures à 32°C) avant le choc thermique (4 heures à 42°C). Un groupe de contrôle est maintenu à 36°C. L’analyse de l’expression relative des protéines issues de l’expérience et des gènes d’immunité est assurée par polymérase en temps réel (qPCR). La mesure au niveau de chaque abeille de la quantité de virus trouvée après un temps d’infection normal de 72 heures est moindre que dans l’échantillon maintenu à température constante, en moyenne de 74% pour le test 1, de 90% pour le 2 et de 87% pour le 3. On mesure bien que l’expression relative des gènes d’immunité et des HSPs montre une corrélation positive, ce qui suggère une corégulation potentielle de ces gènes en réponse aux agents déclencheurs, même si les résultats varient un peu selon les trois expériences distinctes. Mais l’ARN à deux brins, marque caractéristique d’une infection virale, n’a pas suffi pour récapituler le modèle d’induction de HSP généralement observé dans les abeilles infectées par un virus, ce qui indique la nécessité d’interactions entre le virus et l’hôte, au-delà de la reconnaissance du modèle moléculaire, pour entraîner l’expression de quelques gènes codant de HSP dans les abeilles infectées.
Constatations
Ce serait trop long et trop complexe de développer les détails des expériences et des analyses qui ont suivi, mais l’étude est en consultation libre et nous pouvons conclure ce petit compte rendu ainsi : l’étude indique que les protéines de réponse au stress, y compris celles dans le réseau de HSR, participent à la défense antivirale de l’abeille. D’autres futures analyses bio-chimiques devront expliquer comment identifier avec certitude les modes de coordination entre le stress et les protéines de défense immunitaire, mais aussi les autres fonctions antivirales de ces protéines, voire déterminer s’il existe une interaction directe ou non avec des protéines virales. Bref, on ne sait pas encore très bien comment ça marche, ni encore totalement pourquoi ça marche, mais on a vérifié que cela marchait, ce qui n’était jusqu’alors qu’une hypothèse vraisemblable. Les chercheurs vont continuer à trouver, mais les praticiens aussi, qui pourront peut-être un jour prochain nous indiquer des conseils pratiques, c’est-à-dire comment mieux aider simplement nos abeilles à se défendre contre ces virus.
Simonpierre DELORME ()
- Viruses, revue mensuelle à comité de lecture, est publiée par MDPI. Y sont affiliées les sociétés de virologie
américaine, australienne, allemande, brésilienne, suédoise, espagnole, canadienne et italienne : www.mdpi.com/journal/viruses - Alexander J. McMenamin, Katie F. Daughenbaugh & Michelle L. Flenniken : « The Heat Shock Response in the Western Honey Bee (Apis mellifera) is antiviral », Viruses, 2020, Feb 22 : https://pubmed.ncbi.nlm.nih.gov/32098425/
- Christiana M. Grozinger (Penn State) & Michelle L. Flenniken (Montana State) : « Bee Viruses: Ecology, Pathogenicity, and Impacts », Annual Review of Entomology, 2019, 64, 205–226.
https://www.annualreviews.org/doi/10.1146/annurev-ento-011118-111942 - COMMENT AMÉLIORER SON IMMUNITÉ
- Philip T. Starks, Caroline A. Blackie, Thomas D. Seeley (Section of Neurobiology and Behavior, Cornell University, Ithaca, NY) : « Fever in honeybee colonies », Naturwissenschaften (2000), DOI: 10.1007/s001140050709, https://pubmed.ncbi.nlm.nih.gov/10883439/
- Révision : fiche Wikipedia « Maladies de l’abeille »
- www.aujardin.info/fiches/bourdon-des-pierres.php
- Vidéo : https://vimeo.com/538892445
Cet article a été initialement publié dans la revue Abeilles & fleurs N°837 en Mai 2021.
